Оставить заявку
Для заказа и получения более подробной информации оставьте заявку, наш менеджер свяжется с Вами!
Нажимая на кнопку, вы даете согласие на обработку персональных данных и соглашаетесь c политикой конфиденциальности
Обнаружение дефицита фосфора с помощью гиперспектральной визуализации для ранней характеристики бессимптомного роста и фотосинтетических симптомов у кукурузы.
1 Отделение биологических наук, Факультет науки, Университет Принца Сонгклы, Сонгкхла 90110, Таиланд; sutee.k@psu.ac.th
2 Отделение физических наук, Факультет науки, Университет Принца Сонгклы, Сонгкхла 90110, Таиланд; chalongrat.d@psu.ac.th (C.D.); surachet@nairt.or.th (S.W.)
3 Национальный астрономический исследовательский институт Таиланда (публичная организация), Мае Рим, Чиангмай 50180, Таиланд
4 Институт биологических наук, Факультет науки, Университет Малайи, Куала-Лумпур 50603, Малайзия; jingyilau8128@gmail.com (J.Y.L.); acgacheng@um.edu.my (A.C.)
- Корреспонденция: lompong.k@psu.ac.th
Аннотация
Дефицит фосфора (P) severely ограничивает рост и урожайность кукурузы, однако его раннее выявление остается сложной задачей, поскольку видимые симптомы проявляются только после продолжительного голодания. В этом исследовании оценивалась способность гиперспектральной визуализации (HSI) в сочетании с машинным обучением обнаруживать дефицит P у проростков кукурузы как на симптоматической, так и на досимптоматической стадиях. Было проведено два тепличных эксперимента: долгосрочная горшечная система в условиях высокого и низкого содержания P и краткосрочный гидропонный эксперимент с тремя концентрациями фосфата (Pi): 500, 100 и 0 мкмоль/л. После длительного дефицита P наблюдалось значительное снижение биомассы побегов и содержания Pi, в то время как биомасса корней увеличилась, и изменился профиль питательных веществ. Гиперспектральные сигнатуры выявили четкие различия на определенных длинах волн в видимой, красно-граничной и ближней инфракрасной (NIR) областях: листья с дефицитом P показали более низкое отражение в зеленой и NIR областях, но более высокое отражение в красной полосе. Модель машинного обучения на основе многослойного перцептрона достигла 99,65% точности в различении P-обработок. В краткосрочном эксперименте дефицит P значительно снизил содержание Pi в тканях в течение одной недели, не влияя на пигментный состав или параметры фотосинтеза. Несмотря на отсутствие видимых симптомов, гиперспектральные измерения обнаружили тонкие спектральные изменения, особенно в старых листьях, что позволило достичь точности классификации 80,71–84,56% на первой неделе и 85,88–90,98% на второй неделе P-обработки. Обычные вегетационные индексы показали слабую корреляцию с содержанием Pi и не смогли обнаружить ранний дефицит P. Эти результаты демонстрируют, что HSI в сочетании с машинным обучением может эффективно обнаруживать дефицит P до появления видимых симптомов, предлагая неразрушающий, быстрый диагностический инструмент для точного управления питательными веществами в системах производства кукурузы.
Ключевые слова: гиперспектральная визуализация; дефицит фосфора; машинное обучение; раннее обнаружение; кукуруза; многослойный перцептрон; дистанционное зондирование
1. Введение
Дефицит фосфора (P) severely снижает рост кукурузы и урожайность зерна, причем потери урожая составляют от 10 до 60% в зависимости от серьезности и продолжительности дефицита P [1-3]. В ответ на дефицит P растения кукурузы проявляют характерные морфологические адаптации, направленные на повышение эффективности поглощения P. Эти адаптации включают увеличение соотношения биомассы корня к побегу, стимуляцию развития боковых корней и корневых волосков, увеличение экссудации органических кислот и фосфатаз, а также формирование симбиотических ассоциаций с микоризными грибами [4,5]. Эти адаптивные реакции представляют собой скоординированное перепрограммирование развития, которое отдает приоритет распределению ресурсов в подземную часть для максимизации способности к поглощению P. Однако, несмотря на эти адаптивные механизмы, продолжительный дефицит P неизбежно приводит к замедлению роста, уменьшению площади листьев, задержке созревания и существенным потерям урожая. Поэтому раннее выявление дефицита P позволяет своевременно проводить корректирующие вмешательства, такие как целенаправленное внесение удобрений, до появления видимых симптомов. Этот упреждающий подход минимизирует физиологический ущерб и предотвращает потери урожая, гарантируя, что растения поддерживают адекватный уровень P на протяжении критических стадий роста.
Классические симптомы дефицита P включают развитие темно-зеленой окраски листьев, часто сопровождаемой пурпурным или красноватым обесцвечиванием, особенно по краям листьев и на нижней стороне листьев. Это красное или пурпурное обесцвечивание является результатом накопления антоциана, которое вызывается нарушением метаболизма углеводов и накоплением избыточных сахаров в условиях ограничения P [6]. При severe дефиците P листья желтеют (хлороз) и наблюдается их старение, причем более старые листья проявляют хлороз по мере того, как P мобилизуется для поддержки более молодых, активно растущих тканей [1]. Эти изменения пигментации напрямую влияют на фотосинтетическую активность. Таким образом, дефицит P fundamentally нарушает работу фотосинтетического аппарата. Более того, P является важным компонентом АТФ и НАДФН, переносчиков энергии, необходимых для светозависимых реакций фотосинтеза [7]. В условиях дефицита P квантовый выход фотосистемы II (Phi2), который представляет эффективность преобразования энергии света в фотохимии, обычно снижается, указывая на нарушение фотосинтетического электронного транспорта. В то же время, когда фотосинтетический аппарат больше не может эффективно использовать улавливаемую световую энергию, непрямое тушение флуоресценции (PhiNPQ) часто увеличивается, поскольку растения рассеивают поглощенную световую энергию в виде тепла, чтобы предотвратить фотоповреждение [7-10].
Кроме того, дефицит P fundamentally изменяет профиль питательных веществ в тканях растений. Самым прямым изменением является существенное снижение как содержания неорганического фосфата (Pi), так и общей концентрации P в тканях [10,11]. Это истощение P неравномерно по всем тканям, поскольку P предпочтительно мобилизуется из старых листьев для поддержки более молодых, активно растущих органов, что приводит к крутым градиентам концентрации P в зависимости от возраста листа и стадии развития [9,10]. Важно отметить, что дефицит P также значительно влияет на накопление и распределение других минеральных питательных веществ через сложные взаимодействия в поглощении, транспорте и утилизации [12]. Дефицит P нарушает минеральный гомеостаз, вызывая увеличение поглощения серы, железа и цинка для компенсации метаболических корректировок, включая ремоделирование липидов. Однако чрезмерное накопление железа и цинка может вызвать токсичность, влияя на общее развитие растений. Эти скоординированные изменения элементного состава тканей отражают взаимосвязанную природу минерального питания растений и центральную регуляторную роль P в метаболическом гомеостазе [13]. Изменения химического состава листьев, вызванные доступностью внутреннего P, создают разнообразный набор сигнатур, которые потенциально могут быть обнаружены и идентифицированы с помощью гиперспектральной визуализации (HSI).
Измененное содержание фотосинтетических пигментов и старение листьев из-за дефицита P создают четкие картины отражения, которые позволяют различать P-статус листьев с помощью гиперспектрального анализа. Предыдущие исследования продемонстрировали эти спектральные изменения у разных видов сельскохозяйственных культур и на разных стадиях развития. В гидропонных экспериментах с рисом дефицит P увеличил старение старых листьев, причем листья с дефицитом P демонстрировали более высокое отражение в видимой области, но более низкое отражение в ближней инфракрасной (NIR) области по сравнению с листьями с достаточным количеством P [14]. Последующее исследование, включавшее как молодые, так и старые полностью развернутые листья риса, показало, что разные уровни P приводят к различному содержанию фотосинтетических пигментов с соответствующими возрастными различиями в картинах отражения [10]. У кукурузы листья с дефицитом P развивали пурпурное обесцвечивание на краю листа, сопровождаемое снижением вегетационных метрик, включая нормализованный разностный вегетационный индекс (NDVI), индекс отражения антоциана (ARI) и потенциальный индекс биоразнообразия (PBI). Отражение как в видимой, так и в NIR области было выше у листьев с дефицитом P, чем у листьев с достаточным количеством P. Видоспецифичные реакции отражения на различное внесение P удобрений были задокументированы у сельдерея, сахарной свеклы и клубники, где разные уровни P приводили к различному содержанию фотосинтетических пигментов и соответствующим спектральным различиям [15]. Однако эти исследования были сосредоточены на обнаружении дефицита P, когда присутствовали видимые симптомы, такие как старение листьев и деградация пигментов. Критический пробел в знаниях остается относительно ранних стадий дефицита P, когда растворимый Pi и общий Pi в листьях снижаются без изменений в фотосинтетических пигментах или видимых симптомах.
Настоящее исследование было разработано для оценки способности HSI определять P-статус листьев кукурузы, с особым акцентом на раннее обнаружение до появления видимых симптомов или значительных физиологических изменений. Мы предположили, что снижение содержания Pi и общего P в листьях, вызванное дефицитом P, генерирует отличительные гиперспектральные сигнатуры, которые могут быть охарактеризованы даже тогда, когда обычные методы оценки, такие как визуальный осмотр и стандартные вегетационные индексы, не позволяют идентифицировать стресс, вызванный недостатком питательных веществ. Здесь мы провели два тепличных эксперимента: долгосрочное горшечное исследование, в котором проростки кукурузы выращивались в контрастных условиях высокого P (HP) и низкого P (LP) в течение шести недель для создания хорошо выраженных симптомов дефицита P и спектральных сигнатур, и краткосрочное гидропонное исследование, в котором проростки подвергались воздействию различных концентраций P в течение одной-двух недель для отслеживания раннего прогрессирования дефицита P до появления видимых симптомов. Мы подтвердили реакции растений на нескольких уровнях: от параметров роста целого растения и пигментного состава листьев до специфического для тканей содержания Pi и измерений фотосинтетической эффективности. Спектры гиперспектрального отражения были получены от листьев на разных стадиях развития и проанализированы с использованием статистических методов и алгоритмов классификации машинного обучения для выявления дискриминационных спектральных особенностей и оценки точности классификации.
2. Материалы и методы
2.1. Растительный материал и дизайн экспериментов
2.1.1. Эксперимент 1: Долгосрочный дефицит фосфора в горшечной системе
Семена кукурузы проращивали на влажной фильтровальной бумаге в течение пяти дней в темноте и пересаживали в 2-литровые горшки, содержащие смесь песка, перлита и торфяного мха (8:1:1, об./об./об.). В каждом горшке находился один проросток (n = 14 биологических повторностей). Проростки орошали 100 мл дистиллированной воды дважды в день и удобряли 200 мл половинного раствора Хогланда, содержащего либо 0,5 ммоль/л NH₄H₂PO₄ (HP), либо 0,5 ммоль/л NH₄Cl (LP), три раза в неделю в течение шести недель. Эксперимент проводился с мая по июль 2025 года. Погодные условия во время эксперимента регистрировались с помощью регистратора данных RK600-07 (Rika Electronic Tech Co., Ltd., Чанша, Китай). Средняя температура и относительная влажность составляли 31,9 ± 1,6°C и 77,3 ± 10,8% соответственно.
2.1.2. Эксперимент 2: Краткосрочный дефицит фосфора в гидропонной системе
Семена кукурузы проращивали в течение трех дней на влажной фильтровальной бумаге в темноте. Всего 72 проростка кукурузы были отобраны для гидропонного выращивания в полистирольных ящиках, по шесть проростков на ящик. Каждый ящик содержал 4 литра 0,5× раствора Хогланда и поддерживался в открытой теплице в течение одной недели. Уровень воды в гидропонной системе контролировался ежедневно, и гидропонные растворы полностью заменялись два раза в неделю. Через одну неделю растения обрабатывали тремя различными концентрациями P: 0, 100 и 500 мкмоль/л NH₄H₂PO₄ в 0,5× растворе Хогланда, с четырьмя ящиками на обработку P (n = 4 биологических повторности). Обработки были обозначены как NP (нет P), LP и HP. Содержание аммония в гидропонных растворах выравнивали с помощью NH₄Cl. На 7 и 14 дни после начала обработки по два растения (2 технические повторности) из каждого ящика были отобраны для анализа. Погодные условия регистрировались во время эксперимента с помощью регистратора данных RK600-07 на месте (Rika Electronic Tech Co., Ltd., Чанша, Китай). Средняя температура и относительная влажность составляли 29,5 ± 1,9°C и 92,2 ± 9,1% соответственно.
2.2. Измерение параметров роста кукурузы
Регистрировали количество листьев и длину побегов собранных растений. Затем образцы побегов и корней отбирали и высушивали в печи при 70°C в течение трех дней для определения сухого веса с помощью аналитических весов (±0,0001 г, MET24T, METTLER TOLEDO, Грайфензее, Швейцария). На верхушке растения самый последний появившийся, полностью развернутый лист был определен как первый лист (Лист 1), представляющий молодую ткань листа. Третий и четвертый листья ниже Листа 1 (Лист 3 и Лист 4) представляли более старую ткань листа.
2.3. Измерение фотосинтетических пигментов
Для измерения фотосинтетических пигментов приблизительно 20 мг свежей ткани листа из молодого или старого листа помещали в микроцентрифужные пробирки. В каждую пробирку добавляли один миллилитр 80% (об./об.) ацетона, и образцы хранили в темноте при 4°C в течение одной недели. Абсорбцию супернатантов измеряли при 470, 647 и 664 нм с использованием спектрофотометра (SPECTROstar Nano, BMG LABTECH, Ортенберг, Германия). Концентрации хлорофилла a, хлорофилла b и каротиноидов рассчитывали в соответствии с [16].
2.4. Измерение фотосинтетических параметров
Фотосинтетические параметры измеряли с помощью флуорометра MultispeQ (PhotosynQ, Ист-Лансинг, Мичиган, США). Измерения проводились в средней части листа Листа 1 и Листа 4 в условиях окружающего освещения. Измеряемые параметры включали квантовый выход фотосистемы II (Phi2), выход непрямого тушения флуоресценции (PhiNPQ) и выход нерегулируемого рассеяния энергии (PhiNO). Phi2 представляет долю поглощенной световой энергии, используемой для фотохимии в ФСII, со значениями от 0 до 1, где более высокие значения указывают на более эффективное использование света для фотосинтеза. PhiNPQ представляет долю поглощенной световой энергии, рассеиваемой в виде тепла посредством регулируемых фотопротекторных механизмов, а PhiNO представляет долю световой энергии, теряемой в результате нерегулируемых процессов [17].
2.5. Определение содержания неорганического фосфата в листьях и корнях
Для определения концентрации Pi в тканях растений использовали количественный анализ на основе молибденового синего [18]. Приблизительно 20 мг ткани собирали с Листа 1, Листа 4 и корней. Образцы ткани гомогенизировали с помощью микропестика в 600 мкл 3% (об./об.) HClO₄ в микроцентрифужных пробирках объемом 1,5 мл. Гомогенат центрифугировали при 12 000 × g в течение 10 минут при комнатной температуре. Затем 120 мкл супернатанта смешивали с 80 мкл аналитического реагента, состоящего из 1% (вес/об.) молибдата аммония, содержащего 50 г/л FeSO₄·7H₂O. Смесь инкубировали при 37°C в течение 2 минут. После инкубации абсорбцию измеряли при 720 нм с помощью планшетного ридера (SPECTROstar Nano, BMGLABTECH, Ортенберг, Германия). Содержание неорганического фосфора (Pi) определяли путём сравнения со стандартной кривой, построенной с использованием KH2PO4 в диапазоне 5–600 нмоль/мл.
2.6. Определение концентрации и содержания питательных веществ
2.6. Определение концентрации и содержания питательных веществ Сухие образцы побегов из разных P-обработок были проанализированы на содержание макро- и микроэлементов (n = 7 биологических повторностей). Общий C и N определяли методом сухого сжигания с использованием анализатора C/N (CN628, LECO Corporation, Сент-Джозеф, Мичиган, США) в соответствии с [19]. Для определения других питательных веществ 0,5 г измельченного сухого образца побега подвергали кислотному разложению с 2 мл 65% (об./об.) HNO₃ и инкубировали при 95°C в течение 1 часа. Затем добавляли 1 мл 30% (об./об.) H₂O₂, и смесь дополнительно инкубировали при 95°C в течение 30 минут для обеспечения полного разложения. Разложенный образец фильтровали через фильтровальную бумагу Whatman № 1 и доводили до 10 мл деионизированной водой. Общий P, K, Ca, Mg, Cu, Mn, Fe, Mo, B и Zn определяли с помощью inductively coupled plasma optical emission spectrometry (ICP-OES) согласно официальным методам AOAC [20,21]. Общий Cl определяли волюметрическим титрованием [22], а общую S измеряли турбидиметрически с помощью спектрофотометра (Spectroquant® Prove 300, Merck KGaA, Дармштадт, Германия). Содержание питательных веществ рассчитывали как произведение концентрации питательного вещества в экстракте и сухого веса побега.
2.7. Статистический анализ
Анализ данных выполнялся с использованием статистического программного обеспечения R версии 4.5.1 [23]. Значительные различия между обработками анализировались с помощью однофакторного дисперсионного анализа (ANOVA) с последующим пост-тестом LSD в пакете Agricolae [24]. Анализ главных компонент (PCA) был выполнен для сравнения моделей накопления питательных веществ в листьях проростков кукурузы между обработками HP и LP. Биплоты были построены с 95% доверительными эллипсами вокруг групп обработок. Визуализация данных выполнялась с помощью пакета ggplot2 [25].
2.8. Гиперспектральная визуализация
Была разработана HSI-система на основе призмы-решетки (grism) для получения спектров отражения, связанных с физико-химическими свойствами, образцов листьев кукурузы. Подробные описания HSI-оборудования, а также соответствующие процедуры спектральной и пространственной калибровки, проведенные перед сбором данных, доступны в [26]. Система охватывает спектральный диапазон 450-850 нм со спектральным разрешением 2 нм и обеспечивает пространственное разрешение приблизительно 0,5 мм. Для долгосрочного горшечного эксперимента HSI-изображения были получены от целых побегов кукурузы. В краткосрочном гидропонном эксперименте листья кукурузы помещали на черные акриловые пластины, установленные на жестком предметном столике, как показано на Рисунке 1A. Равномерное двустороннее освещение достигалось с помощью широкополосных источников света в видимой-NIR области, состоящих из 100 Вт, 5000 K светодиодных панелей (LCFOCUS, Шэньчжэнь, Китай) и 400 Вт, 3300 K галогенных ламп (Shenzhen Tezelong Technology, Шэньчжэнь, Китай), расположенных симметрично для избежания теней. Рабочее расстояние между образцом и передней линзой системы составляло 3,2 м для получения достаточно большого поля зрения, позволяющего визуализировать несколько листьев за одно сканирование. Гиперспектральные данные собирались с использованием конфигурации сканирования pushbroom, реализованной с помощью вращающегося сканирующего механизма, работающего с угловой скоростью 3,5 мрад/с, что соответствует линейной скорости сканирования приблизительно 1,12 см/с на плоскости объекта.
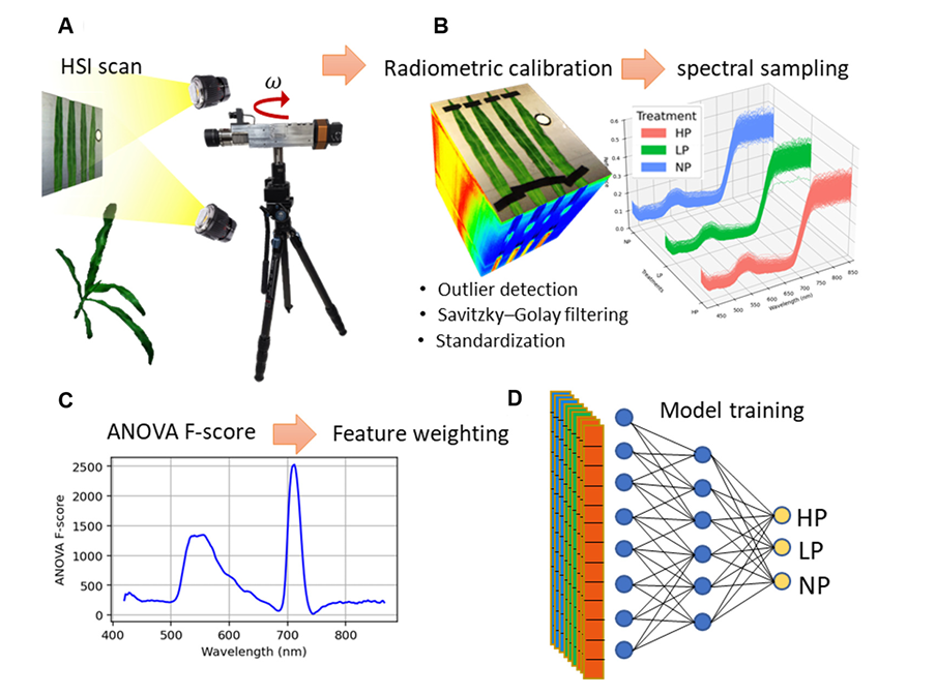
Рисунок 1. Схема анализа с использованием гиперспектральной визуализации (HSI) для классификации статуса фосфора в листьях кукурузы.
Гиперспектральные данные были получены с листьев кукурузы с помощью сканирующей системы HSI на основе grism-спектрометра с конфигурацией pushbroom (A). Конвейер предварительной обработки данных начинался с радиометрической калибровки для преобразования исходной интенсивности в коэффициент отражения и включал спектральную предобработку: обнаружение выбросов с помощью z-критерия, фильтрацию Савицкого–Голея для снижения шума и стандартизацию данных. Был проведён балансировкой выборки (n = 10 000 спектров на класс) для трёх классов обработки: HP (500 мкмоль/л Pi), LP (100 мкмоль/л Pi) и NP (без фосфора, 0 мкмоль/л Pi) (B). Далее выполнялся анализ признаков на основе дисперсионного анализа (ANOVA) с отображением распределения F-критерия по длинам волн для выявления дискриминационных спектральных областей, после чего проводилось взвешивание признаков для усиления информативных длин волн (C). Архитектура нейронной сети многослойного перцептрона (MLP) для классификации состояла из входного слоя, соответствующего количеству спектральных диапазонов, двух скрытых слоёв (128 и 64 нейрона с функцией активации ReLU) и выходного слоя softmax для прогнозирования трёх классов фосфорной обработки (D).
2.8.2. Спектральная предварительная обработка и отбор данных
Область интереса (ROI) на листьях была вручную отделена от фона, и спектры всех пикселей ROI были извлечены и сохранены в виде двумерного массива спектральных векторов [N_пиксель, N_полос] с соответствующими метками обработок, записанными в одномерном массиве. Для получения чистого и сбалансированного набора данных для анализа был применен многоэтапный конвейер спектральной предварительной обработки. Во-первых, в пределах каждого класса P-обработки аномальные спектры удалялись с использованием метода обнаружения выбросов на основе z-оценки [28]. Для каждого спектра R_i(c)(λ) в классе c z-оценка вычислялась для каждой длины волны, и спектры, удовлетворяющие max_λ(|z_i(λ)|) > 5, исключались для удаления аномальных измерений, вызванных шумом, ошибками сегментации или паразитными отражениями. Все оставшиеся спектры были очищены от шума с использованием фильтра Савицкого-Голея [29] для сохранения узких полос поглощения при одновременном снижении высокочастотного шума. Для получения равномерно распределенного набора данных, подходящего для машинного обучения, из каждого класса обработок было случайным образом отобрано 10 000 спектров. Это привело к сбалансированному набору данных отражения R_i(c)(λ), i = 1, ..., 10 000, c ∈ {HP, LP, NP}.
Для каждого эксперимента приблизительно 75% биологических повторностей были отнесены к обучающему набору, а оставшиеся 25% - к тестовому набору, гарантируя, что все спектры из данной повторности попадают исключительно в один поднабор. В долгосрочном горшечном эксперименте с дефицитом фосфора (n = 14 биологических повторностей) растения (горшки) были разделены на обучающий набор (n = 10) и тестовый набор (n = 4). В краткосрочном гидропонном эксперименте с дефицитом фосфора (n = 8 биологических повторностей) повторности были разделены на обучающий набор (n = 6) и тестовый набор (n = 2).
Для каждого класса обработок спектры отражения случайным образом отбирались на уровне пикселей из нескольких полностью развернутых листьев всех биологических повторностей в каждом поднаборе. Сбалансированный набор данных из 10 000 спектров на класс был создан, причем 7500 спектров были взяты из обучающего поднабора и 2500 спектров независимо из тестового поднабора.
2.8.3. Расчеты вегетационных индексов
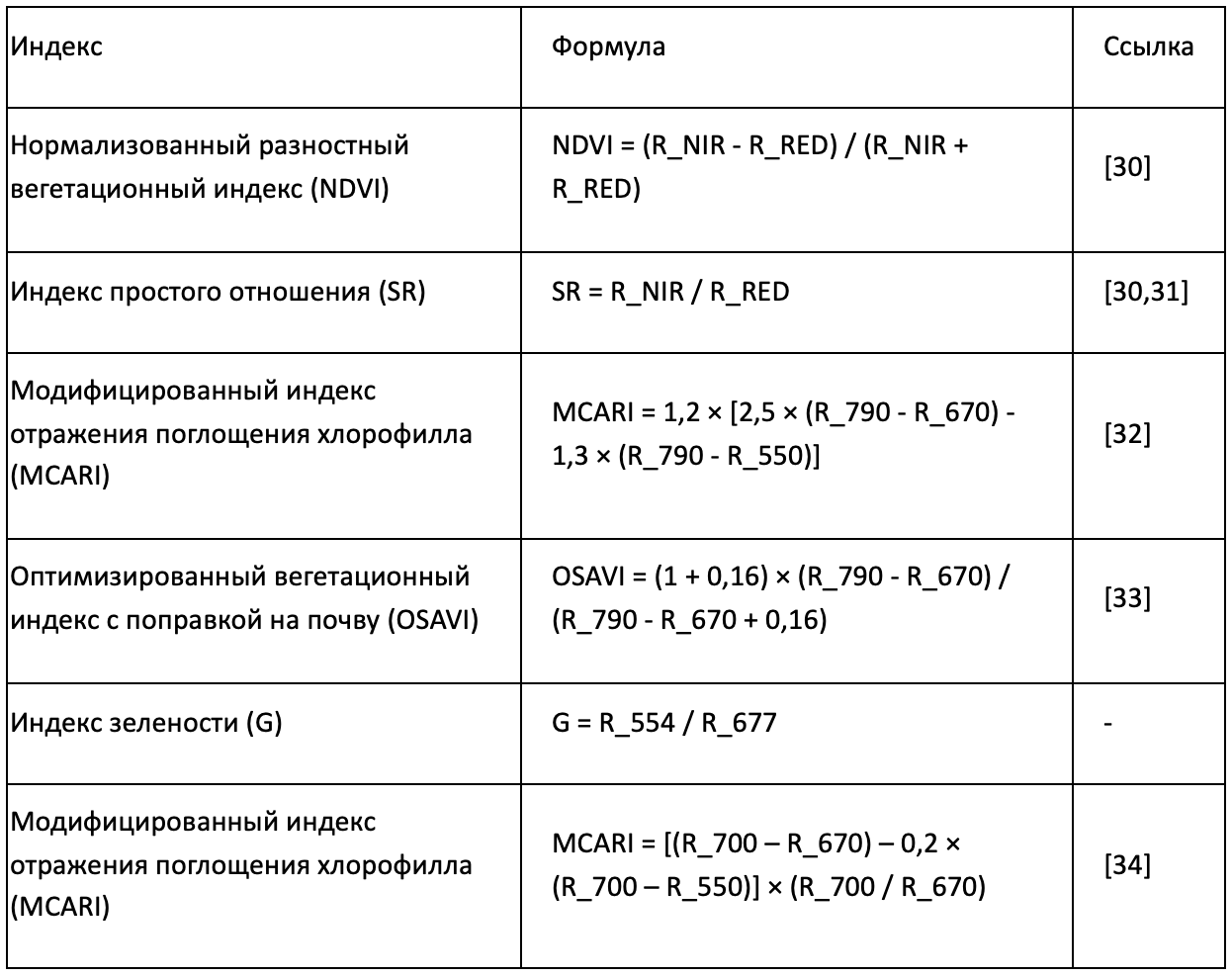
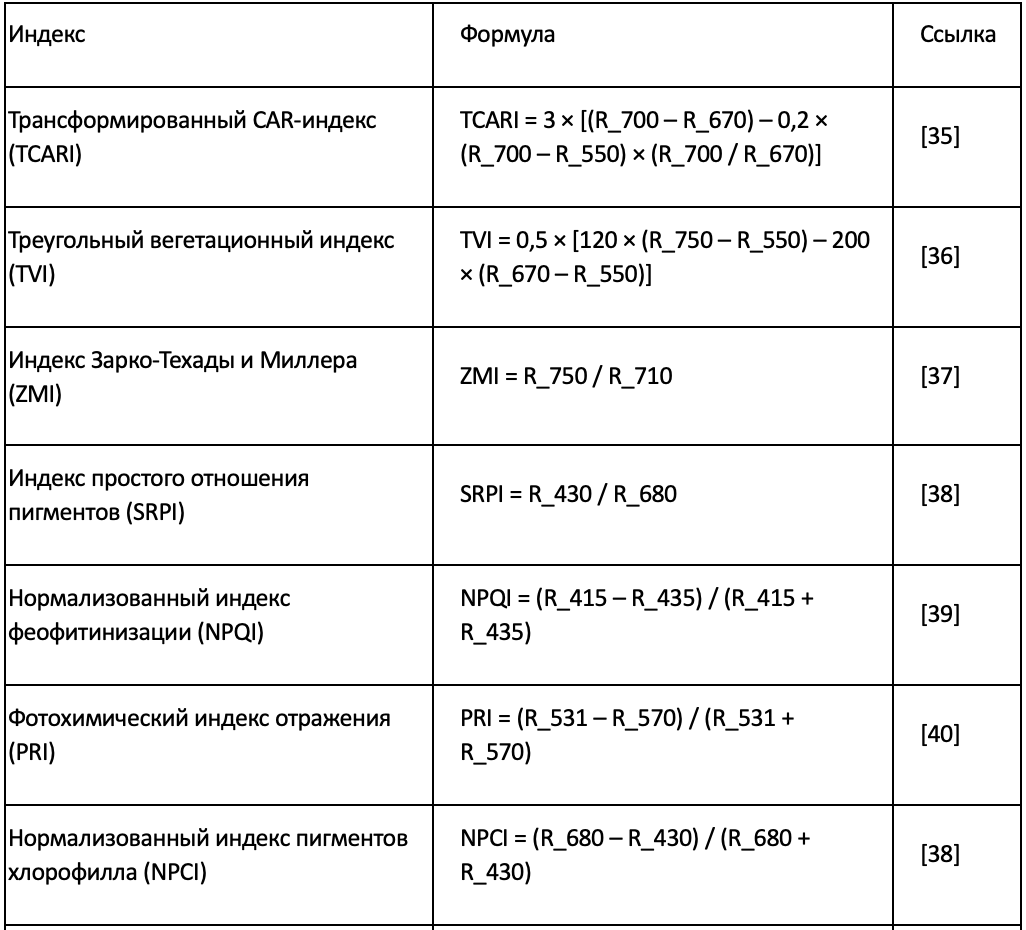
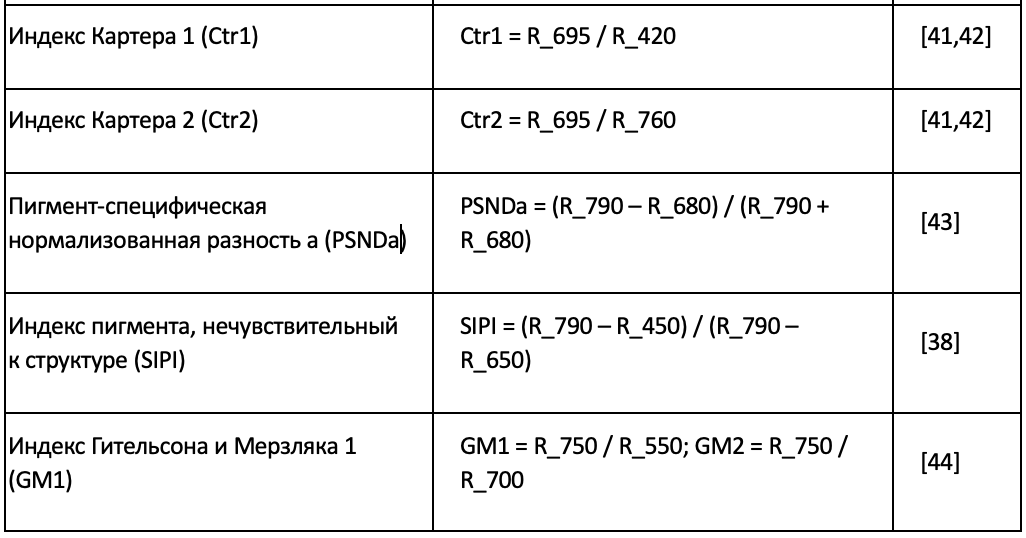
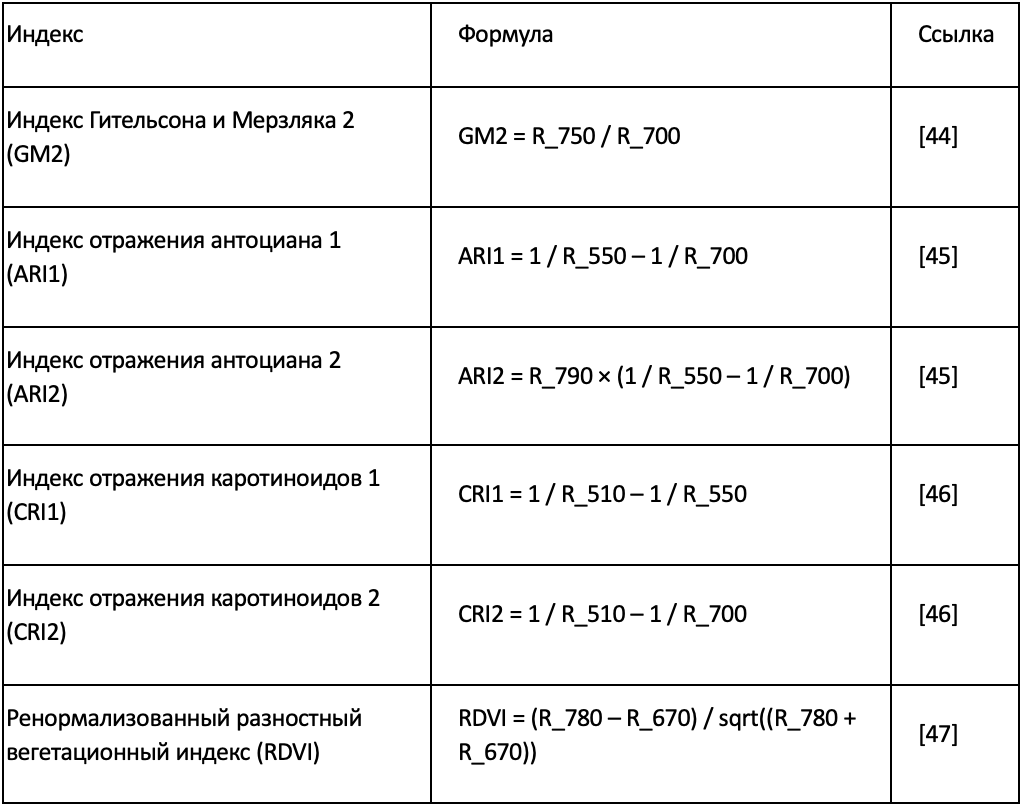
Вегетационные индексы рассчитывались с использованием среднего спектра гиперспектрального отражения для каждой группы образцов. Образцы группировались в соответствии с возрастом листа (Лист 1 и Лист 4), временем измерения (одна и две недели после обработки) и P-обработкой (HP, LP и NP). Для каждой группы все спектры, принадлежащие к одной комбинации возраста листа, времени и обработки, усреднялись для получения репрезентативного среднего спектра. Затем значения отражения на требуемых длинах волн извлекались из этого среднего спектра, и вегетационные индексы вычислялись с использованием стандартных формул (Таблица 1). Рассчитанные индексы охватывали зеленый цвет, поглощение хлорофилла, пигментный состав и структурные характеристики, что позволяло последовательно сравнивать спектральные реакции в зависимости от обработок и стадий развития листьев.
Таблица 1. Список рассчитанных вегетационных индексов.
2.8.4. ANOVA F-оценка для анализа признаков
Чтобы оценить дискриминационный вклад каждой спектральной длины волны в разделение классов P-обработок, мы вычислили F-оценку однофакторного ANOVA как функцию длины волны. Для каждой длины волны λ F-оценка количественно определяла отношение между дисперсией среднего отражения классов и дисперсией внутри каждого класса. F-статистика на длине волны λ была определена как в [48]:
F(λ) = [ Σ_c=1^C n_c (R̄(c)(λ) - R̄(λ))² / (C - 1) ] / [ Σ_c=1^C Σ_i=1^n_c (R_i(c)(λ) - R̄(c)(λ))² / (N - C) ], (2)
где R_i(c)(λ) - отражение образца i, принадлежащего классу c, на длине волны λ; R̄(c)(λ) - среднее отражение класса c; а R̄(λ) - глобальное среднее по всем образцам. В этом исследовании C = 3 было количеством классов обработок; n_c = 10 000 было количеством спектров на класс; и N = 30 000, общее количество спектров по всем обработкам. Пример F(λ) показан на Рисунке 1C. Более высокие значения F(λ) указывают на длины волн, где спектральные различия между классами P-обработок велики по сравнению с внутриклассовой изменчивостью, тем самым выделяя информативные спектральные области для дискриминации P-статуса. Все F-оценки были вычислены с использованием функции f_classif из библиотеки Scikit-Learn Python версии 1.8.0.
2.8.5. Обучение модели MLP
Для классификации уровней P-обработки непосредственно по тонким изменениям в измерениях полносигнального отражения была обучена нейронная сеть MLP с использованием предварительно обработанного и сбалансированного спектрального набора данных. Перед обучением модели был применен дополнительный этап взвешивания признаков на основе F-оценки ANOVA для усиления вклада информативных спектральных полос. F-оценки были нормализованы до диапазона [0, 1],
F̃(λ) = (F(λ) - F_min) / (F_max - F_min), (3)
и спектры отражения были преобразованы поэлементным взвешиванием:
R_i(c)(λ)_weighted = R_i(c)(λ) * F̃(λ). (4)
Затем все взвешенные спектры были стандартизированы с использованием
R_i(c)_scaled(λ) = (R_i(c)(λ)_weighted - μ(λ)) / σ(λ), (5)
где μ и σ обозначают среднее значение и стандартное отклонение для каждой длины волны, вычисленные по обучающему поднабору. Эта схема взвешивания сохраняет полную спектральную размерность, функционируя как механизм мягкого внимания, улучшая стабильность классификатора и уменьшая влияние низкоинформативных спектральных областей.
Классификация выполнялась с использованием MLP с прямой связью, реализованного в MLPClassifier из Scikit-Learn, с входным слоем, соответствующим количеству волновых полос, двумя скрытыми слоями из 128 и 64 нейронов с активацией ReLU и выходным слоем softmax, представляющим классы HP, LP и NP. Модель обучалась с использованием оптимизатора Adam. Переобучение контролировалось с помощью комбинации регуляризации весов L2 (α = 10⁻⁴), ранней остановки после 20 эпох без улучшения валидации и взвешивания признаков на основе F-оценки для подавления вкладов от низкоинформативных длин волн. Пятикратная стратифицированная перекрестная проверка использовалась для оценки надежности, при этом средняя точность перекрестной проверки обеспечивала несмещенную оценку производительности. Окончательная оценка модели проводилась на отложенном тестовом наборе с использованием общей точности и нормализованной по строкам матрицы ошибок для оценки прогностической производительности по каждому классу.
3. Результаты
3.1. Влияние долгосрочного дефицита фосфора на фенотип роста и гиперспектральные сигнатуры проростков кукурузы
На 6-й неделе обработки LP биомасса побегов проростков кукурузы была значительно ниже, чем при обработке HP, но биомасса корней была значительно выше (Рисунок 2A). Сухой вес побегов был приблизительно на 40% ниже в условиях LP, в то время как сухой вес корней был на 29% выше. Количество функциональных листьев также было значительно ниже у растений с дефицитом P (Рисунок 2B), хотя количество нефункциональных листьев существенно не различалось между двумя обработками.
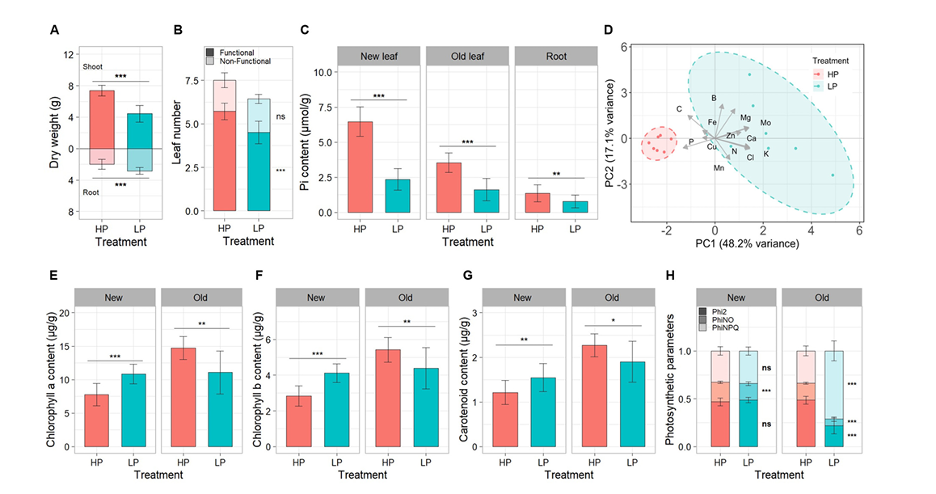
Рисунок 2. Влияние дефицита фосфора на биомассу, параметры роста, накопление пигментов и фотосинтез у проростков кукурузы в условиях горшечной культуры. Проростки кукурузы выращивались в течение шести недель в условиях высокого содержания фосфора (HP) и низкого содержания фосфора (LP). (A) Сухой вес побегов и корней. (B) Количество листьев, включая как функциональные, так и нефункциональные листья. (C) Концентрация неорганического фосфата (Pi) в Листе 1 (новый лист), Листе 4 (старый лист) и корнях. (D) Анализ главных компонент (PCA) накопления питательных веществ. (E–G) Фотосинтетические пигменты: хлорофилл a, хлорофилл b и каротиноиды. (H) Фотосинтетические параметры: Phi2, PhiNPQ и PhiNO. Данные представлены как средние значения ± SD (n = 14). Для сравнения обработок HP и LP использовался t-критерий Стьюдента (ns = не значимо; *p < 0,05; **p < 0,01; ***p < 0,001).
Цитозольный Pi и общая концентрация P подтвердили успешное создание условий дефицита P. Содержание Pi было значительно ниже у растений LP во всех исследованных тканях (Рисунок 2C). Лист 1 показал наиболее выраженное снижение концентрации Pi, в то время как Лист 4 и ткани корней также продемонстрировали значительное снижение содержания Pi. Кроме того, общее содержание P в биомассе побегов проростков кукурузы снизилось приблизительно на 55% в условиях LP (Таблица S1). PCA накопления питательных веществ в биомассе побегов проростков кукурузы выявило четкую кластеризацию между обработками HP и LP (Рисунок 2D), при этом PC1 объяснял 48,2% дисперсии, а PC2 - 17,1% дисперсии. Характер разделения показал, что P-голодание изменило общий профиль питательных веществ со значительными изменениями в накоплении P, N, K, Ca, Mg, Mo, Zn и Cl (Таблица S1).
Содержание фотосинтетических пигментов было значительно затронуто обработкой LP. Содержание хлорофилла a в Листе 1 было выше в условиях LP, в то время как содержание хлорофилла a в Листе 4 было выше у растений с достаточным количеством P (Рисунок 2E). Хлорофилл b и каротиноиды демонстрировали аналогичную картину: концентрации пигментов были выше в Листе 1 при обработке LP, но выше в Листе 4 при обработке HP (Рисунок 2F, G). Параметры фотосинтетической эффективности выявили различные реакции на дефицит P в зависимости от стадии развития листа (Рисунок 2H). При обработке LP Phi2 был значительно снижен в Листе 4, но PhiNPQ увеличился. Напротив, эти параметры не показали различий между обработками HP и LP в Листе 1. Эти результаты указывают на то, что дефицит P изменяет содержание фотосинтетических пигментов и ухудшает фотосинтетическую активность зависящим от возраста листа образом.
Результаты гиперспектрального анализа побегов проростков кукурузы выявили четкие различия на определенных длинах волн между обработками HP и LP. В зеленой области (∼540–560 нм) листья сдефицитом P демонстрировали немного более низкое отражение, чем листья с достаточнымколичеством P. В желтой области (∼540–610 нм) листья LP показали более низкое отражение, чтосогласуется с потерей каротиноидов в Листе 4 (Рисунок 2G). Напротив, в красной полосе (∼620–680 нм) наблюдалось стабильно более высокое отражение у листьев LP, что напрямую отражаетзначительные снижения хлорофилла a и b, количественно определенные в старых листьях LP (Рисунок 2E, F). Этот более мелкий красный провал является прямым оптическим следствием потерипигмента. Перемещаясь в красно-граничную область (700–740 нм), листья LP показали более слабый наклон по сравнению с листьями HP, что соответствует комбинированным эффектам сниженного хлорофилла и нарушенной фотосинтетической эффективности, на что указывают более низкие значения Phi2 и более высокие PhiNPQ у старых листьев LP (Рисунок 2H). Наконец, в NIR-области (∼760–850 нм) листья LP демонстрировали более низкое отражение, что согласуется с уменьшеннымвнутренним рассеянием, вызванным сниженной целостностью мезофилла и меньшим накоплениембиомассы.
Эти явные спектральные различия позволили модели MLP крайне точно классифицировать P-обработки. Как показано на Рисунке 3B, модель достигла общей точности 99,65%, что указывает на высокую разделимость спектральных признаков между обработками в контролируемых условиях. Эта высокая производительность в первую очередь обусловлена долгосрочной обработкой дефицитом фосфора, которая вызвала выраженные физиологические и структурные изменения в листьях, что привело к четко различимым спектральным сигнатурам, особенно по форме и наклону в видимой, красно-граничной и ближней инфракрасной областях. Однако, поскольку спектры анализировались на уровне пикселей, это значение следует интерпретировать как верхнюю границу оценки точности классификации. Тем не менее, этот результат демонстрирует чувствительность гиперспектральной визуализации к лежащим в основе различиям в пигментном составе, фотосинтетической эффективности и структурной целостности.
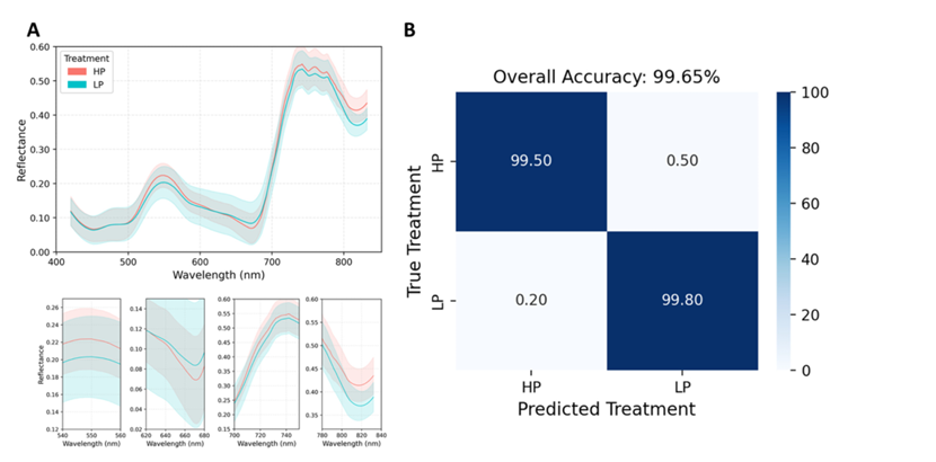
Рисунок 3. Сигнатуры гиперспектрального отражения и эффективность классификации для дискриминации статуса фосфора.** Спектры гиперспектрального отражения от побегов проростков кукурузы в условиях высокого и низкого содержания фосфора (обработки HP и LP) (A). Сплошные линии представляют среднее отражение, а заштрихованные области указывают стандартное отклонение (n = 14). На расширенных панелях под полными спектрами показаны детальные картины отражения в определенных областях длин волн. Матрица ошибок от классификации многослойным перцептроном (MLP) показывает точность различения двух P-обработок (B). Значения представляют процент образцов из каждой истинной обработки (строки), правильно классифицированных в предсказанные категории (столбцы)
.2. Реакции роста и гиперспектральные реакции проростков кукурузы на краткосрочный дефицит фосфора
Гидропонные эксперименты проводились в 0,5× растворе Хогланда, дополненном тремя концентрациями Pi: 0, 100 и 500 мкмоль/л NH₄H₂PO₄. На 7-й день не наблюдалось значительных различий в сухом весе побегов, сухом весе корней и количестве листьев между обработками, что указывает на то, что эффекты дефицита P еще не проявились в морфологических признаках (Рисунок 4A-C). Однако на 14-й день появились явные различия по всем измеренным параметрам. Сухой вес побегов был значительно ниже в обработке NP по сравнению с обработками LP и HP (Рисунок 4A). Напротив, сухой вес корней демонстрировал противоположную картину. Проростки в обработке NP имели значительно большую биомассу корней - в 1,93 и 1,19 раза больше, чем в обработках HP и LP, соответственно (Рисунок 4B). Развитие листьев также было заметно затронуто доступностью P. На 14-й день общее количество листьев было меньше в обработке NP, с видимым старением нижних листьев. Напротив, проростки в обработках HP и LP сохраняли приблизительно девять функциональных листьев без наблюдаемого старения (Рисунок 4C). Эти результаты показывают, что дефицит P не только подавляет образование новых листьев, но и ускоряет старение существующих фотосинтезирующих тканей.
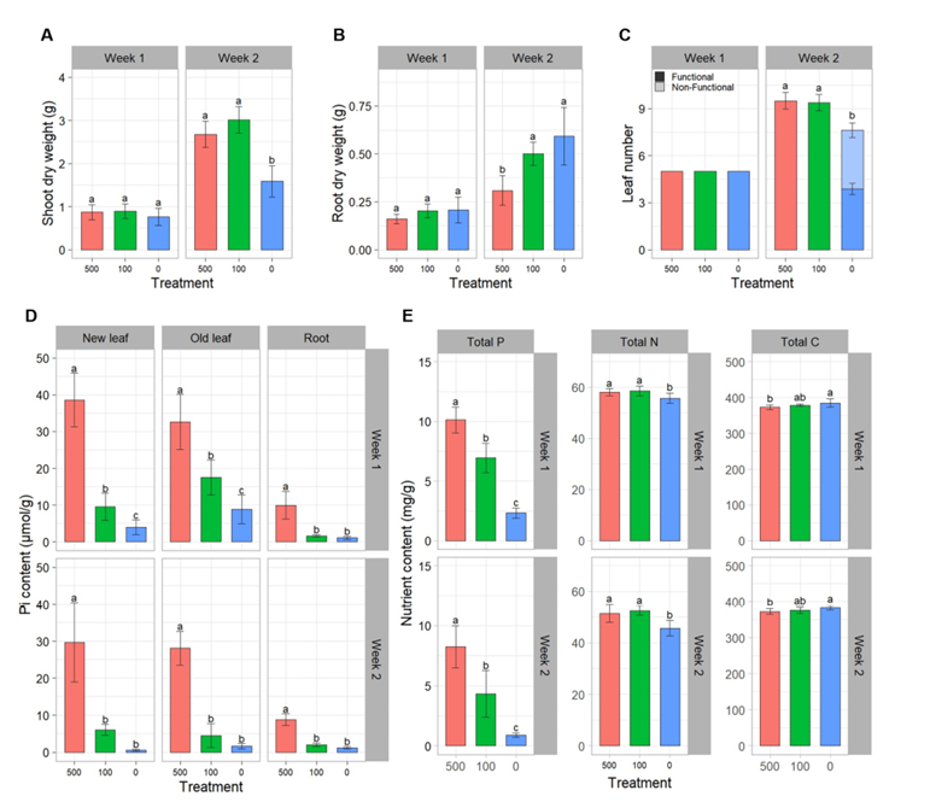
Рисунок 4. Морфологические и физиологические реакции проростков кукурузы на краткосрочный дефицит фосфора.** Проростки кукурузы выращивались гидропонно в течение 1 недели на 500 мкМ Pi, а затем на 500, 100 и 0 мкМ Pi перед определением фенотипов роста. Измеренные параметры роста включали сухой вес побегов (A), сухой вес корней (B) и количество листьев (C). Для количества листьев листья визуально классифицировались как функциональные (темные столбцы) или нефункциональные (светлые столбцы) на основе их зелености. Содержание Pi (D) измерялось в первом и четвертом полностью развернутых листьях и в корнях. Общий P, N и C в побегах проростков кукурузы (E) были количественно определены. Данные представлены как средние значения ± SD (n = 8). Различные буквы указывают на статистически значимые различия между обработками при p < 0,05 на основе однофакторного ANOVA с последующим тестом LSD.
Чтобы выяснить, влияет ли количество доступного Pi на распределение Pi по разным органам растения и стадиям развития, мы количественно определили содержание Pi в Листе 1 и Листе 4. На 7-й день все три типа тканей демонстрировали значительные различия в накоплении Pi в зависимости от обработки. Как в Листе 1, так и в Листе 4 содержание Pi соответствовало градиенту внешнего поступления: самые высокие уровни - в обработке HP, промежуточные - в LP и самые низкие - в NP. Ткань корней показала значительно более низкое накопление Pi, чем листья, во всех обработках (Рисунок 4D). Общее содержание P в побегах показало значительные эффекты обработки в оба срока сбора урожая, следуя градиенту внешнего поступления Pi (Рисунок 4E). Более того, общее содержание N в побегах было значительно выше в обработках HP и LP по сравнению с обработкой NP (Рисунок 4E). И наоборот, общее содержание C в побегах показало обратную зависимость от поступления P. Значительно больше углерода накопилось в обработке NP, чем в LP, в то время как обработка HP продемонстрировала самое низкое содержание C в оба срока сбора (Рисунок 4E).
Кроме того, чтобы оценить, влияет ли доступность Pi на эффективность использования питательных веществ и стехиометрический баланс, мы рассчитали эффективность использования фосфора (PUE), соотношение N:P и соотношение C:P (Рисунок S2). PUE была значительно выше в обработке NP в оба временных точки, что указывает на повышенную эффективность производства биомассы в условиях ограниченной доступности Pi (Рисунок S2A). Соотношения N:P и C:P также были заметно выше в обработке NP с самыми высокими соотношениями, наблюдаемыми на 14-й день, в то время как растения с достаточным количеством P поддерживали значительно более низкие соотношения (Рисунок S2B,C). Эти результаты показывают, что доступность внешнего Pi регулирует не только накопление P, но и fundamentally изменяет баланс N и C у проростков кукурузы, подчеркивая центральную роль P в координации гомеостаза питательных веществ всего растения и метаболического баланса.
Чтобы оценить, изменяет ли дефицит P состав фотосинтетических пигментов, мы количественно определили содержание хлорофилла a, хлорофилла b и каротиноидов и измерили фотосинтетические параметры в новых и старых листьях проростков кукурузы на 7 и 14 дни P-обработки (Рисунок S3). Содержание хлорофилла a, хлорофилла b и каротиноидов оставалось сходным во всех обработках Pi как в новых, так и в старых листьях в оба временных точки (Рисунок S3A-C). На 14-й день не было различий в Phi2, PhiNO и PhiNPQ между новыми и старыми листьями (Рисунок S3D). Эти результаты показывают, что краткосрочный дефицит P не вызывал видимых симптомов, таких как хлороз или деградация пигментов, даже если растворимый P и общий P в листьях были значительно снижены. Отсутствие видимых симптомов дефицита P в листьях в краткосрочной перспективе подчеркивает сложность раннего обнаружения стресса, вызванного недостатком питательных веществ, с помощью обычной визуальной оценки и выделяет потенциальную ценность HSI для обнаружения тонких физиологических и биохимических изменений, которые предшествуют развитию видимых симптомов.
Впоследствии мы предположили, что определенные вегетационные индексы, полученные в результате мультиспектрального анализа, могут различать P-статус в листьях до появления видимых симптомов или фотосинтетических изменений. Особый интерес представляли индексы, чувствительные к тонким биохимическим и структурным изменениям. Корреляционный анализ между вегетационными индексами и содержанием Pi в листьях выявил различные картины, которые зависели от возраста листа и времени (Рисунок S4A). Большинство вегетационных индексов показали слабую или умеренную корреляцию с содержанием Pi как в молодых, так и в старых листьях проростков кукурузы на 7 и 14 дни P-обработки. Более того, корреляции не были последовательными для разного возраста листьев и временных точек. Среди 24 исследованных индексов фотохимический индекс отражения (PRI) продемонстрировал значительные эффекты обработки, причем значения прогрессивно снижались от HP к LP к NP обработкам (Рисунок S4B). Таким образом, вегетационные индексы, полученные из мультиспектрального отражения, не смогли идентифицировать P-статус листьев на ранней стадии дефицита P.
Затем были охарактеризованы гиперспектральные сигнатуры новых и старых листьев. Измерения гиперспектрального отражения на 7-й день выявили относительно тонкие спектральные реакции на доступность P, которые зависели от возраста листа (Рисунок 5A, B). В новых листьях различия между
тремя P-обработками были незначительными при рассмотрении стандартных отклонений; однако картины, специфичные для обработки, стали различимы на расширенных спектральных видах. Новый лист проростков кукурузы, выращенных в условиях NP, давал немного более высокие значения отражения в красной (620-680 нм) и NIR (780-840 нм) областях и более пологий красно-граничный наклон (700-740 нм), в то время как листья обработки HP сохраняли наиболее глубокое поглощение хлорофилла и самый крутой красно-граничный переход (Рисунок 5A). Напротив, старый лист демонстрировал более выраженное разделение обработок, особенно в видимом диапазоне: листья проростков из обработок NP и LP давали большее зеленое отражение (540-560 нм) и более заметное снижение красного поглощения по сравнению с листьями обработки HP. Несмотря на эти более сильные различия в видимых полосах, NIR (780-840 нм) демонстрировала сходную величину и характер разделения обработок как в новых, так и в старых листьях, что указывает на то, что снижение или исключение Pi оказало минимальное влияние на структурное рассеяние в NIR на этой стадии (Рисунок 5B). В целом, эти результаты показывают, что признаки раннего дефицита P обнаруживаются как в новых, так и в зрелых листьях, но изменения в видимых полосах и красно-граничной области более сильно выражены в старых листьях, что согласуется с более ранним началом физиологического стресса и мобилизации питательных веществ.
На 14-й день P-обработки гиперспектральное отражение выявило значительно более сильное разделение в зависимости от обработки, чем наблюдалось на первой неделе, отражая прогрессирование дефицита P. В Листе 1 различия между обработками, которые были незначительными на первой неделе, стали четко выраженными в видимом, красно-граничном и NIR-диапазонах. Листья обработки NP демонстрировали более мелкое красное поглощение (620-680 нм), визуально более пологий красно-граничный наклон (700-740 нм) и повышенное NIR-отражение (780-840 нм), в то время как листья HP сохраняли более глубокие черты пигментного поглощения (Рисунок 5C). На этой стадии старые листья показали еще большее разделение обработок, что согласуется с более ранней реакцией старых тканей на дефицит P. Более того, стандартные отклонения были шире, что указывает на гетерогенное прогрессирование стресса и раннее старение.
Распределения F-оценок ANOVA определили длины волн, которые лучше всего различали обработки HP, LP и NP. На 7-й день P-обработки были обнаружены четкие различия между новыми и старыми листьями (Рисунок S5A, B). В новых листьях доминирующий пик дискриминации приходился на красно-граничную область вблизи 700 нм, что указывает на то, что эта длина волны была наиболее чувствительна к тонким ранним физиологическим различиям между обработками. Вторичный пик присутствовал в зелено-желтом диапазоне (500-600 нм), отражая mild изменения в пигментном поглощении, в то время как NIR-область показала ограниченную дискриминационную способность. Старые листья продемонстрировали существенно более высокие F-оценки в видимой области, особенно от 500 до 650 нм, что согласуется с более выраженными спектральными изменениями, связанными с пигментами, в старых тканях. Красно-граничная область оставалась самым сильным дискриминатором, в то время как NIR-длины волн снова вносили минимальный вклад. Эти картины подтверждают, что старые листья обеспечивают более сильное спектральное разделение во время ранней фазы дефицита P, причем красно-граничная область служит основным индикатором. На 14-й день распределения F-оценок ANOVA показали явный сдвиг в длинах волн, которые вносили наибольший вклад в разделение обработок (Рисунок 5C, D).
Результаты классификации подчеркивают способность HSI в сочетании с машинным обучением различать P-статус листьев на ранней стадии реакции на доступность Pi (Рисунок 6). На 7-й день модель MLP достигла общей точности 80,71% для новых листьев и 84,56% для старых листьев. Эти результаты показывают, что тонкие спектральные различия, особенно в старых листьях, уже можно использовать для классификации статуса питательных веществ до появления любых видимых симптомов. На 14-й день эффективность классификации была выше, показав точность 85,88% для новых листьев и 90,98% для старых листьев. Эта тенденция согласуется с усилением физиологических эффектов дефицита P и увеличением спектрального разделения, наблюдаемого в F-оценках ANOVA.
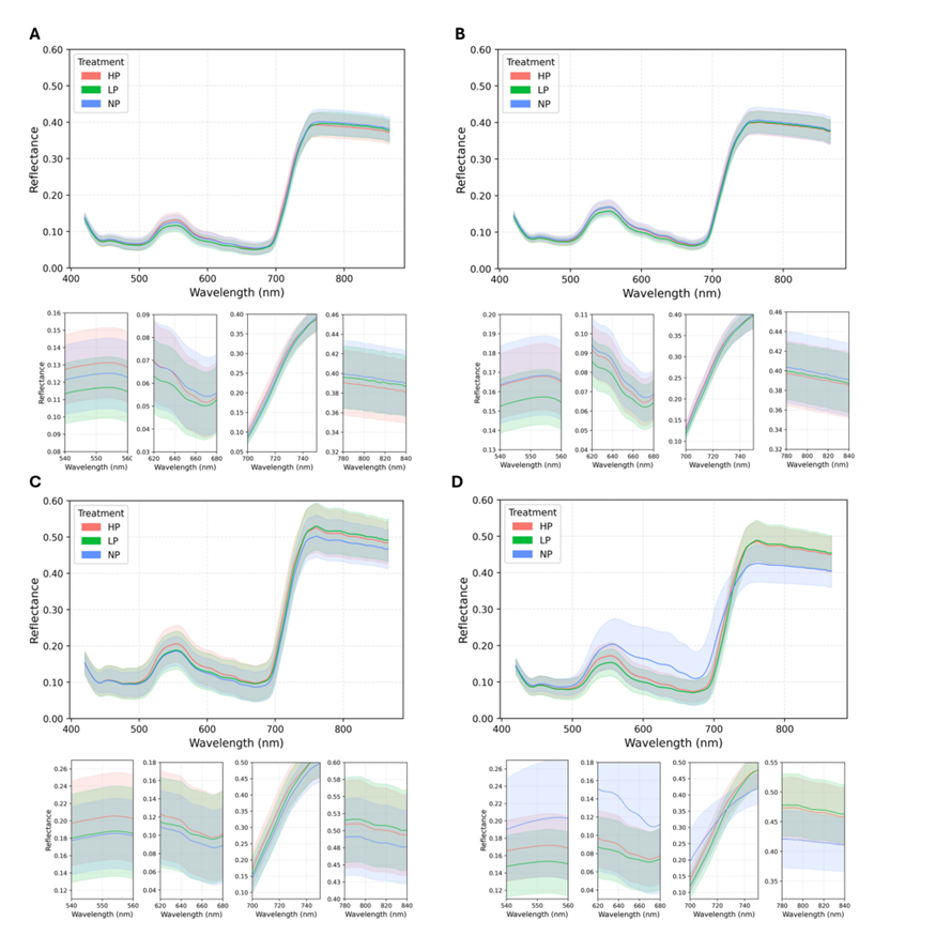
Рисунок 5. Сигнатуры гиперспектрального отражения новых и старых листьев кукурузы при различных обработках фосфором. Средние спектры гиперспектрального отражения (400–850 нм) от новых (A, C) и старых (B, D) листьев проростков кукурузы, выращенных в условиях высокого (HP), низкого (LP) и отсутствия (NP) фосфора в течение 1 недели (A, B) и 2 недель (C, D). На расширенных видах под полными спектрами показаны спектры в четырех ключевых областях длин волн: 540–560 нм, 620–680 нм, 700–740 нм и 780–840 нм. Заштрихованные области представляют стандартные отклонения (n = 8).
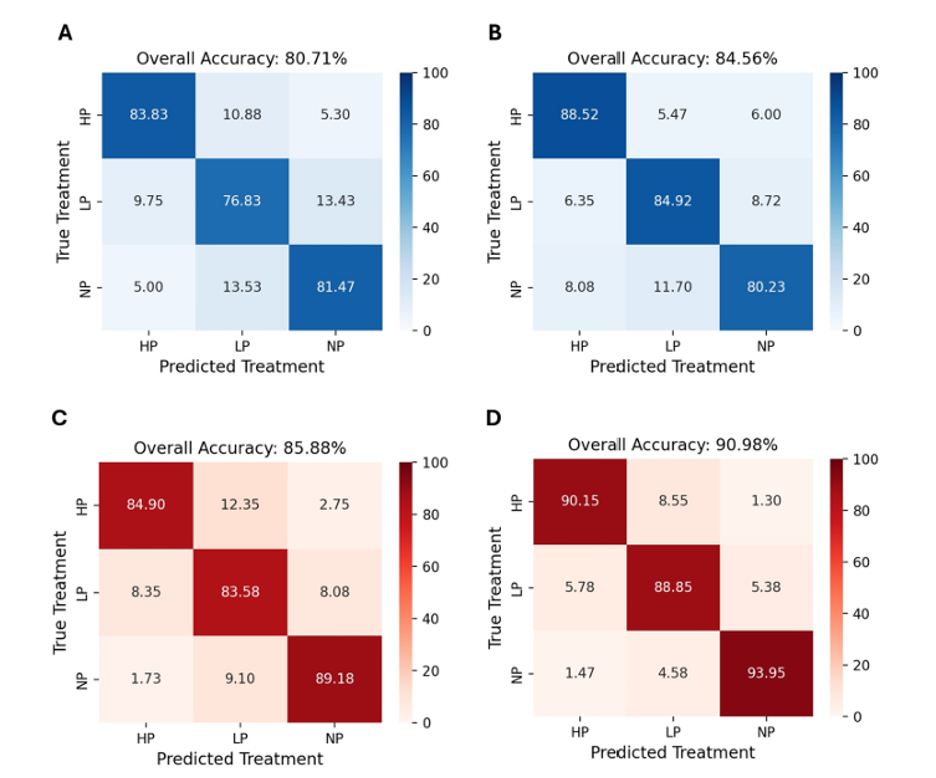
Рисунок 6. Матрицы ошибок классификации MLP для дискриминации статуса фосфора в листьях проростков кукурузы. Эффективность классификации для обработок с высоким (HP, 500 мкмоль/л Pi), низким (LP, 100 мкмоль/л Pi) и отсутствием (NP, 0 мкмоль/л Pi) фосфора на основе гиперспектральных сигнатур новых (A) и старых листьев (B) проростков кукурузы после одной недели обработки и новых (C) и старых листьев (D) после двух недель обработки. Значения в каждой ячейке представляют процент образцов из истинной обработки (строки), предсказанных для каждого класса обработки (столбцы). Диагональные значения указывают на правильные показатели классификации.
4. Обсуждение
4.1. Обнаружение симптомов дефицита P в листьях кукурузы при долгосрочном дефиците с помощью гиперспектральной визуализации
Наши результаты показывают, что HIS высокоэффективна для обнаружения симптомов дефицита P у проростков кукурузы, подвергнутых длительному P-голоданию. После шести недель выращивания в условиях низкого содержания P растения кукурузы проявляли выраженные морфологические и физиологические изменения, которые четко отражались в их гиперспектральных сигнатурах. 40%-ное снижение биомассы побегов в сочетании с 29%-ным увеличением биомассы корней, наблюдаемое в условиях дефицита P (Рисунок 2A), отражает адаптивную стратегию, при которой растения отдают приоритет развитию корней для улучшения поглощения питательных веществ, когда доступность P в почве ограничена. Эта модификация характера роста широко сообщается для культур с дефицитом P и представляет собой фундаментальный механизм реакции на стресс [9,10,49].
Значительное снижение цитозольного Pi и общего содержания P во всех тканях подтвердило полное создание условий дефицита P, причем новый полностью развернутый лист показал наиболее выраженное снижение концентрации Pi (Рисунок 2C). Эта тканеспецифичная реакция подчеркивает динамическую природу перераспределения P внутри растения, при этом более молодые ткани потенциально поддерживают более высокие концентрации P за счет ремобилизации из старых листьев [9,50,51]. Анализ PCA накопления питательных веществ показал, что P-голодание fundamentally изменило общий профиль питательных веществ со значительными изменениями не только P, но и накопления N, K, Ca, Mg, Mo, Zn и Cl (Рисунок 2D и Таблица S1). Эти изменения с участием многих питательных веществ подчеркивают взаимосвязанную природу минерального питания растений и предполагают, что дефицит P вызывает каскадные эффекты на накопление других основных элементов у кукурузы, что согласуется с выводами Schluter et al. (2013) [12].
Зависящие от возраста листа реакции в содержании фотосинтетических пигментов и параметрах фотосинтетической эффективности дают важное понимание того, как дефицит P по-разному влияет на листья на разных стадиях развития (Рисунок 2E-H). Увеличение хлорофилла a, хлорофилла b и каротиноидов в новом полностью развернутом листе в условиях низкого P в отличие от снижения в старом листе предполагает, что молодые листья поддерживают или усиливают свою фотосинтетическую способность в качестве компенсаторного механизма, в то время как старые листья испытывают деградацию пигментов и старение [9,10]. Значительное снижение Phi2 и повышение PhiNPQ в старых листьях с дефицитом P указывает на нарушение фотосинтетической эффективности и увеличение рассеивания энергии в виде тепла, отражая пагубные последствия продолжительного дефицита P для фотосинтетического аппарата [9,10,12].
Гиперспектральные сигнатуры улавливали эти сложные физиологические изменения с замечательной чувствительностью. HIS обнаружил более низкое отражение в зеленой области (540-560 нм) у листьев с дефицитом P (Рисунок 3A). Это спектральное изменение согласуется со спектрами отражения листьев банана на ранней стадии грибковой инфекции Pseudomonas fujisensis, что соответствует заболеванию на адаксиальной поверхности листьев [52]. Эти структурные изменения подтверждаются наблюдаемыми снижениями биомассы побегов и количества функциональных листьев, а также перемещением питательных веществ из старых тканей (Рисунок 2A-C). Постоянно более высокое отражение в красной полосе (620-680 нм), наблюдаемое у листьев с дефицитом P (Рисунок 3A), напрямую указывает на значительное снижение хлорофилла a и b, количественно определенное в старых листьях, поскольку этот более мелкий провал красного поглощения является прямым оптическим следствием потери пигмента [14,53].
Красно-граничная область (700-740 нм) показала более низкое отражение у листьев с дефицитом P по сравнению с листьями с достаточным количеством P (Рисунок 3A), что соответствует комбинированным эффектам сниженного хлорофилла и нарушенной фотосинтетической эффективности, на что указывают более низкие значения Phi2 и более высокие значения PhiNPQ (Рисунок 2H). Положение и наклон красно-граничной области являются хорошо установленными индикаторами здоровья растительности и содержания хлорофилла, что делает эту спектральную область особенно ценной для обнаружения стресса, вызванного недостатком питательных веществ [54]. Более низкое отражение, демонстрируемое листьями с дефицитом P в NIR-области (780-840 нм), согласуется с уменьшенным внутренним рассеянием, вызванным сниженной целостностью мезофилла и меньшим накоплением биомассы [14,55]. NIR-плато в первую очередь определяется внутренней структурой листа, и его снижение в условиях дефицита P отражает кумулятивные эффекты деградации тканей и снижения биомассы [56].
Точность модели MLP, составившая 99,65% для классификации обработок с высоким и низким содержанием P, демонстрирует мощь сочетания HIS с машинным обучением для оценки статуса питательных веществ (Рисунок 3B). Эта почти идеальная производительность отражает чувствительность гиперспектральных признаков к лежащим в основе изменениям пигментного состава, фотосинтетической эффективности и структурной целостности, которые сопровождают долгосрочный дефицит P [10,14,54]. Способность достигать такой точной дискриминации также подчеркивает потенциал HIS в качестве неразрушающего, быстрого и надежного инструмента для диагностики дефицита P в системах производства кукурузы, предлагая явные преимущества по сравнению с традиционной визуальной оценкой или деструктивным анализом тканей.
4.2. Характеристика листьев кукурузы с дефицитом P на ранней стадии дефицита
Раннее обнаружение дефицита P представляет собой критическую задачу в точном земледелии, поскольку видимые симптомы, такие как изменение пигментации листьев и старение листьев, обычно появляются только после продолжительного периода P-голодания [9,10]. После одной недели P-обработки не наблюдалось значительных различий в параметрах роста, включая сухой вес побегов, сухой вес корней и количество листьев, что указывает на то, что ранние эффекты дефицита P еще не проявились в признаках ростовой активности (Рисунок 4A-C). Однако анализ содержания Pi в тканях выявил значительные различия в зависимости от обработки во всех исследованных тканях, согласуются с более ранним началом стресса, вызванного дефицитом P, и активными процессами мобилизации питательных веществ в старых тканях [10,61]. Эти различные спектральные реакции позволили точно классифицировать P-статус с помощью машинного обучения.
Наши результаты демонстрируют временное прогрессирование эффектов дефицита P на гиперспектральные сигнатуры и точность классификации машинного обучения в листьях проростков кукурузы. В течение первой недели дефицита P, когда видимые симптомы отсутствовали, модель MLP достигла точности 80,71% в новых листьях и 84,56% в старых листьях (Рисунок 6A, B). На этой бессимптомной стадии дефицит P в первую очередь вызывает биохимические изменения, включая снижение содержания P и перебалансировку питательных веществ, наряду с ремоделированием мембранных липидов, характеризующимся увеличением не-фосфорных липидов и уменьшением фосфолипидов [12,62]. Ко второй неделе, по мере того как дефицит P усиливался и вступал в раннюю симптоматическую стадию, точность классификации существенно улучшилась до 85,88% и 90,98% в молодых и старых листьях, соответственно (Рисунок 6C, D). Это улучшение отражает прогрессирование структурных изменений и изменений, связанных с пигментами, включая деградацию мезофилла, потерю хлорофилла и старение тканей, которые создают сильные спектральные сигнатуры в нескольких областях длин волн [10]. Эти результаты подчеркивают потенциал HSI в сочетании с машинным обучением для раннего, неразрушающего мониторинга P-статуса, одновременно указывая на то, что чувствительность обнаружения увеличивается по мере того, как физиологический стресс прогрессирует от биохимических к структурным проявлениям.
5. Выводы
Наше исследование демонстрирует, что гиперспектральная визуализация в сочетании с машинным обучением обеспечивает мощный, неразрушающий подход для обнаружения дефицита P у кукурузы как на симптоматической, так и на досимптоматической стадиях. Дефицит P индуцирует отличительные спектральные сигнатуры в видимой, красно-граничной и ближней инфракрасной областях, которые отражают лежащие в основе изменения пигментного состава, фотосинтетической эффективности и структурной целостности листа. У растений с долгосрочным дефицитом P модель многослойного перцептрона достигла исключительной точности классификации (99,65%), подтверждая высокую чувствительность гиперспектральных признаков к стрессу, вызванному дефицитом P. Что более важно, мы демонстрируем, что гиперспектральная визуализация может обнаружить ранний дефицит P у кукурузы до появления видимых симптомов или значительных изменений в фотосинтетических пигментах. В течение первых двух недель P-голодания, когда содержание Pi в тканях и общее содержание P были значительно снижены, но уровни хлорофилла и фотосинтетические параметры оставались неизменными, гиперспектральные измерения улавливали тонкие спектральные реакции, которые обеспечивали точную классификацию, что представляет собой значительный прогресс по сравнению с обычными вегетационными индексами и методами визуальной оценки. Старые листья постоянно демонстрировали более сильные спектральные сигнатуры из-за более раннего начала стресса и активной мобилизации питательных веществ, а красно-граничная область (700–740 нм) служила особенно чувствительным ранним индикатором, в то время как видимая и ближняя инфракрасная области становились все более дискриминационными по мере прогрессирования истощения P. Будущие исследования должны быть сосредоточены на валидации этого подхода в разнообразных полевых условиях, расширении методологии на другие стадии роста и генотипы кукурузы, а также на разработке практических инструментов поддержки принятия решений для облегчения внедрения в коммерческое производство кукурузы.
Вспомогательные материалы: Следующая вспомогательная информация может быть загружена по адресу: https://www.mdpi.com/article/10.3390/agronomy16080772/s1, Рисунок S1: Дизайн эксперимента и гидропонная установка для проростков кукурузы, выращенных при различных уровнях фосфора (Pi). ... Рисунок S2: Влияние доступности фосфора на эффективность использования фосфата (PUE) и соотношения питательных веществ у проростков кукурузы на ранних стадиях роста. ... Рисунок S3: Влияние дефицита фосфора на накопление пигментов и фотосинтетические параметры у проростков кукурузы, выращенных в гидропонных условиях. ... Рисунок S4: Взаимосвязи между вегетационными индексами и содержанием фосфата (Pi) в листьях, а также влияние обработок на фотохимический индекс отражения (PRI) у кукурузы. ... Рисунок S5: Дискриминационная способность на конкретных длинах волн для классификации статуса фосфора (P). ... Таблица S1: Концентрации питательных веществ в сухой биомассе кукурузы после шести недель горшечной культуры в условиях высокого (HP) и низкого (LP) содержания фосфора.
05 мая / 2026
